復分解反應的三個條件初中 什么是復分解反應
文章目錄[隱藏]
- 1基本介紹
- 2發(fā)生條件
- 三方程記憶指令
- 特別注意
- 5復分解反應概述

文章插圖
復分解反應是四種基本反應類型之一 。復分解反應是兩種化合物相互交換組分產(chǎn)生另外兩種化合物的反應 。復分解反應的本質(zhì)是發(fā)生復分解反應的兩種物質(zhì)在水溶液中交換離子,結合成難以電離的物質(zhì)——沉淀、氣體或弱電解質(zhì)(最常見的是水) 。縮寫為AB+CD→AD+CB 。

文章插圖
1基本介紹復分解反應是化學中四種基本反應類型之一 。要理解它,必須把握概念中“復合”和“交換成分”兩個關鍵詞 。酸、堿和鹽溶液之間的反應通常是由兩種化合物之間的組分交換形成的,即參與復分解反應的化合物在水溶液中電離解離成自由移動的離子,這些離子再結合成新的化合物 。因此,酸、堿和鹽溶液之間的反應通常是復分解反應 。
文章插圖
2發(fā)生條件基本條件:發(fā)生復分解的兩種物質(zhì)在水溶液中可以交換離子,結合成難以電離的物質(zhì)(沉淀、氣體或弱電解質(zhì)) 。

文章插圖
1.堿性氧化物+酸:酸具有強酸性(如HCl、H2SO4、硝酸等) 。)并能做出反應 。
2.酸+堿(中和反應):當酸堿較弱時,不發(fā)生反應 。
3.酸+鹽:強酸生成弱酸;離子交換后有沉淀;與強酸碳酸鹽反應;如果滿足一個條件,就會發(fā)生反應 。
4.堿+鹽:強堿與銨鹽反應;兩種反應物都是可溶的,離子交換后,有沉淀、水和氣體中的一種 。如果滿足一個條件,就會發(fā)生反應 。
5.鹽+鹽:兩種反應物都可以溶解,經(jīng)過離子交換后,會有沉淀、水和氣體中的一種,滿足一個條件就可以發(fā)生反應 。
三方程記憶指令總結以上五類復分解反應能夠發(fā)生并趨于完成的條件,可分為記憶掌握兩個方面 。一方面對反應物的要求:酸式鹽、酸、堿一般可以接受,而鹽鹽、鹽堿則需要溶解;另一方面是對產(chǎn)品的要求:產(chǎn)品中有沉淀或氣體排放,或產(chǎn)生水等弱電解質(zhì) 。正確寫出復分解反應的化學方程式,必須考慮這兩個方面 。
特別注意
注意第一點:
需要注意的是,堿+非金屬氧化物→鹽+水的反應不是復分解反應 。
因為根據(jù)復分解反應的定義 。只有當兩種化合物相互交換組分時,生成兩種新化合物的反應才是復分解反應 。
注意第二點:
酸+金屬氧化物→鹽+水是復分解反應 。
堿+非金屬氧化物→鹽+水,不屬于復分解反應 。
5復分解反應概述復分解反應是兩種化合物交換組分形成另外兩種化合物的反應 。本質(zhì)上,兩種化合物在溶液中交換離子,即同時交換陽離子或陰離子 。縮寫為AB+CD=AD+CB 。
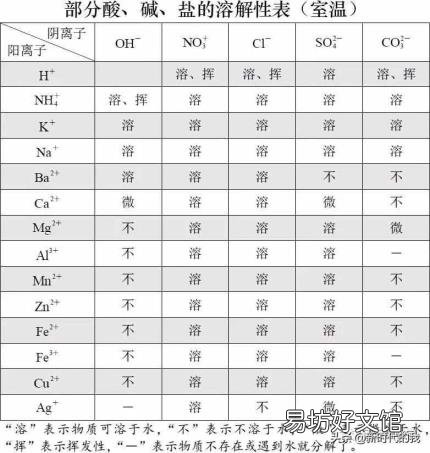
復分解反應的本質(zhì)是溶液中的離子結合成難以電離的物質(zhì)(如水)、難以溶解的物質(zhì)(如沉淀)或揮發(fā)性氣體,復分解反應趨于完成 。為了準確識別復分解反應的發(fā)生,必須熟記常見酸、堿、鹽的溶解度表,正確使用物質(zhì)的溶解度 。
文章插圖
【小貼士】學習是一種成長,思考是一種智慧,反饋是一種美德 。送一朵玫瑰給某人,留一抹余香在手上,分享你所知道的智慧,幫助更多的朋友成長 。
歡迎使用微信微信官方賬號:中學高分征集
【復分解反應的三個條件初中 什么是復分解反應】
推薦閱讀
- fruit常用單數(shù)還是復數(shù) fruit可數(shù)嗎
- 草莓長葉時可以施復合肥嗎
- 小學一年級啊喔鵝拼音字母 九個復韻母是什么
- 盆底肌康復訓練方法是什么?
- 假如今天往一家銀行存10億,明天取走,后天再存,大后天再取走,如此反復,銀行會怎么樣?
- 羊毛衫縮水了輕松復原 羊毛衫縮水了怎么辦
- 蘇州的房價會報復性下跌嗎?
- 痘坑怎么淡化 痘坑如何修復
- 高考數(shù)學復習注意事項合集 數(shù)學高考
- 演員陣容強大到已經(jīng)無法復制的電視劇有哪些?







